- Услуги
- Цена и срок
- О компании
- Контакты
- Способы оплаты
- Гарантии
- Отзывы
- Вакансии
- Блог
- Справочник
- Заказать консультацию
Заказать консультацию
Коллигативные свойства
Снижение химического потенциала растворителя в присутствии растворенного вещества вызывает изменения некоторых физических свойств растворов: давления насыщенного пара, точки кипения, точки замерзания, осмотического давления и др.
Свойства, которые не зависят от природы растворенного вещества, называют коллигативными свойствами раствора. Растворенные вещества – обычно это ионы – имеют эффективную молярность, которая в два или более раз превышает номинальную; эта эффективная концентрация называется осмолярностью.
В качестве растворителя берем только воду, что раствор предельно разбавлен, растворенное вещество нелетуче и не образует с водой твердых растворов.
Индекс 1 будет относиться к растворителю (вода), а 2 – к растворенному веществу. При условии справедливости сделанных допущений снижение давления насыщенного пара над раствором при любой температуре следует из закона Рауля (1.37):

Изменение температуры кипения (∧Tb) при стандартном давлении (1 бар) определяется выражением (1.38):

При выводе уравнения (1.37) сделано ряд допущений вполне допустимых для предельно разбавленных растворов. Необходимо отметить, что величина Е значительно зависит от давления внешней среды. Изменение температуры замерзания обычно описывается уравнением (1.39):

Осмотическое давление (π) раствора может быть интерпретировано как давление, которое нужно приложить к раствору, чтобы увеличить химический потенциал растворителя до значения химического потенциала чистого растворителя при стандартном давлении.
Осмотическое давление проявляется и может быть измерено в случае, если растворитель и раствор отделены друг от друга полунепроницаемой мембраной, которая позволяет проходить молекулам растворителя, а растворенным веществам – нет (рис. 1.5).
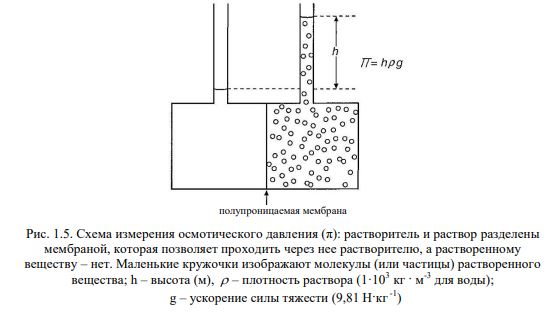
Ясно, что если приложить к раствору внешнее давление, которое выше его осмотического давления, растворитель будет перемещаться в обратную сторону из раствора в отсек с растворителем, тем самым увеличивая концентрацию растворенного вещества; это называется обратным осмосом.
Осмотическое давление предельно разбавленного водного раствора определяется выражением (1.40):

Поскольку m2 = n/V (n – число молей растворенного вещества в объеме V), уравнение (1.40) можно переписать в виде: π *V= nRTV, имеющим тот же вид, что и уравнение состояния идеального газа (1.33).
Интересно
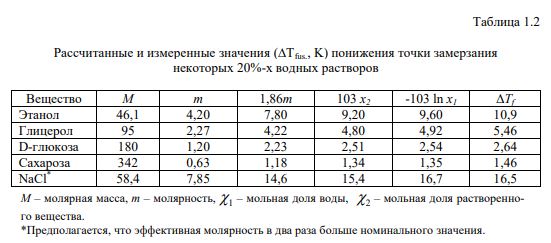
Обоснованность уравнения (1.39), предложенного для расчета понижения точки замерзания воды некоторыми растворенными веществами, проиллюстрирована в таблице 1.2. Видно, что рассчитанные величины хорошо совпадают с экспериментальными, особенно если уравнения используются в их самой строгой форме.
Тем не менее остаются отклонения, которые означают, что при рассматриваемой концентрации растворы уже не являются предельно разбавленными. Сравнение с рис. 1.4 показывает, что для сахарозы отклонения становятся большими при ее концентрации свыше 20 %.
Действительно, уравнения (1.38 1.40) основаны на предложении, что χ1=a1, то есть мольная доля воды в растворе равна ее активности αw.
Если в термодинамических соотношениях (1.38–1.40) заменить величину χ1 величиной αw, которую в большинстве случаев можно измерить, будут получены намного более точные расчетные формулы (ln αw– является коллигативным свойством наряду с другими упомянутыми свойствами).
Для этих целей часто представляется удобным определение точки замерзания. Чтобы избежать ошибок из-за неидеальности растворов, определения должны быть сделаны при нескольких концентрациях и результаты экстраполированы к нулю.
Для определения молярной массы макромолекул предпочтительнее измерение осмотического давления, поскольку существуют мембраны, непроницаемые для макромолекул.Экспериментальные данные позволяют получить хороший результат, несмотря на то, что в системе всегда присутствуют низкомолекулярные растворенные вещества. На практике определяется различие в осмотическом давлении, причем это различие обусловлено только макромолекулами.
Статьи по теме
- Силы внутреннего трения жидкости. Уравнение Ньютона
- Идеальные модели деформирующихся систем
- Основные понятия реологии
- Учение о процессах деформации систем
- Теория абсолютных скоростей реакции
- Температурная зависимость скорости реакции
- Теория Дебая–Хюккеля
- Растворы электролитов при диссоциации
- Самоассоциация и электрическое экранирование
Полезные статьи









Узнайте цену услуг:
Узнай цену консультации
"Да забей ты на эти
дипломы и экзамены!”
(дворник Кузьмич)

