- Услуги
- Цена и срок
- О компании
- Контакты
- Способы оплаты
- Гарантии
- Отзывы
- Вакансии
- Блог
- Справочник
- Заказать консультацию
Заказать консультацию
Химический потенциал компонентов раствора
Важной термодинамической характеристикой компонента многокомпонентной гомогенной системы является его химический потенциал μi , определяемый как парциальная молярная свободная энергия компонента.
Ранее мы определили химический потенциал i-ого компонента системы формулой 1.14:

Зависимость химического потенциала компонента от состава жидкой смеси можно выразить уравнением 1.20:

Следует отметить, что уравнение (1.20) применимо только при стандартном давлении. Активность (ai) i-ого компонента (термодинамическая или действующая концентрация) напрямую связана с его концентрацией.
Если состав раствора выражен в мольных долях компонентов ( χi ), активность (ai) i-ого компонента и его мольная доля ( χi ) в растворе связаны соотношением (1.30):

В этом случае при нулевой концентрации (т. е. при = 0 χi ) величина ai = 0. Для чистого индивидуального вещества ai = 1.
Для растворов, называемых идеальными, активность компонента равна его концентрации, выраженной в мольных долях (χ i). Однако идеальность наблюдается не часто, только для смесей, состоящих из очень схожих соединений.На рис. 1.3а показан пример смеси этанола (2) и воды (1), для которой наблюдаются большие отклонения от идеальности.
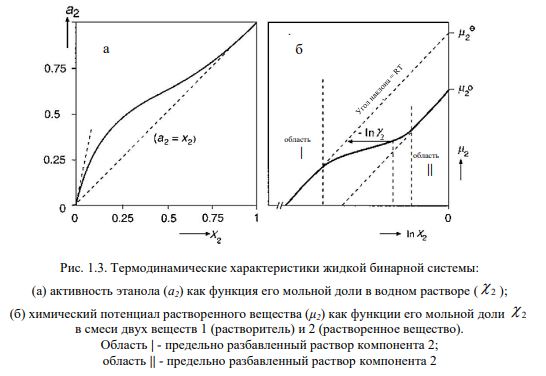
На рис. 1.3а видно, что для разбавленных водных растворов этанола (т. е. если Х2 мала) активность этанола пропорциональна его мольной доле (или концентрации этанола, выраженной иным способом). В этом случае говорят об идеально разбавленном («предельно – разбавленном») растворе.
При небольших значениях Х2 химический потенциал М2 пропорционален величине ln Х2, и угол наклона прямой согласно уравнению (2.20а) равен RT, но линия не экстраполируется к при ln Х2 = 0 (т. е. при Х2 = 1).
При небольших значениях Х2 раствор является предельно разбавленным, химический потенциал растворенного вещества в таком растворе можно выразить формулой (1.31):

Для тех случаев, когда χ не равен α, вводится коэффициент активности (γ), определяемый соотношением (1.30). Коэффициент активности характеризует отклонение системы от идеальной модели. Даже в разбавленных растворах γ часто отклоняется от единицы.
Химический потенциал компонента характеризует его вклад в способность системы изменяться (эволюционировать).
Используя понятие химического потенциала, можно сформулировать представление о движущей силе химической реакции (но не о ее скорости), сформулировать условия химического и фазового равновесия.
Интересно
Так, перенос компонента из одной фазы или части системы в другую всегда будет происходить в направлении более низкого химического потенциала, осуществляется ли перенос диффузией, испарением, кристаллизацией, растворением или каким-либо другим способом.
Активность компонента в большей степени, чем концентрация влияет на его растворимость, диффузию, адсорбцию в поверхностном слое и т.д. Если по каким-то причинам – скажем при добавлении других компонентов – коэффициент активности становится меньше, то активность компонента уменьшается, хотя концентрация остается неизменной.
Статьи по теме
- Силы внутреннего трения жидкости. Уравнение Ньютона
- Идеальные модели деформирующихся систем
- Основные понятия реологии
- Учение о процессах деформации систем
- Теория абсолютных скоростей реакции
- Температурная зависимость скорости реакции
- Теория Дебая–Хюккеля
- Растворы электролитов при диссоциации
- Самоассоциация и электрическое экранирование
Полезные статьи









Узнайте цену услуг:
Узнай цену консультации
"Да забей ты на эти
дипломы и экзамены!”
(дворник Кузьмич)

