- Услуги
- Цена и срок
- О компании
- Контакты
- Способы оплаты
- Гарантии
- Отзывы
- Вакансии
- Блог
- Справочник
- Заказать консультацию
Заказать консультацию
Характеристика первого закона термодинамики
В основе первого закона термодинамики, как и закона сохранения и превращения энергии, лежит принцип эквивалентности различных форм движения материи (видов энергии).
Интересно
Установлено, что различные формы движения материи (тепловая, механическая, электрическая, химическая и т.п.), мерой которых являются количества соответствующих видов работы и теплоты, могут переходить в другие формы в строго определенных, эквивалентных количествах, не зависящих ни от характера процесса преобразования, ни от условий его протекания.
Применительно к термодинамической системе и окружающей среде, которые обмениваются энергией между собой, закон сохранения энергии утверждает, что изменение внутренней энергии системы равно изменению энергии окружающей среды, взятому с обратным знаком.
Работу (независимо от рода) принято считать положительной, если она приводит к уменьшению внутренней энергии системы, то есть работа «совершается» термодинамической системой над окружающей средой.
С учетом правила знаков первый закон термодинамики для изолированной системы может быть математически представлен в следующем виде:
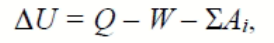
где Q ‒ количество теплоты; W ‒ количество механической работы; Ai ‒ сумма количеств немеханических работ разного рода (электрической, химической и т.п.).
В применении к термомеханической изолированной системе первый закон термодинамики записывается в виде уравнения:
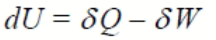
и формулируется следующим образом: изменение внутренней энергии термодинамической системы равно разности между количеством теплоты, подведенной к системе, и количеством механической работы, совершенной системой.
Статьи по теме
- Оценка возможных последствий взрыва для здания и персонала
- Неразрушаемые предохранительные конструкции производственных помещений
- Оценка возможности и целесообразности уменьшения площади разлива
- Оценка возможности снижения аварийной массы горючего вещества
- Оценка последствий детонационного взрыва для смежного объекта
- Оценка последствий взрыва в помещении
- Закон постоянства сумм тепла
- Воздух как окислитель во взрывоопасных воздушных смесях
- Основное уравнение процесса и энтальпия
Полезные статьи









Узнайте цену услуг:
Узнай цену консультации
"Да забей ты на эти
дипломы и экзамены!”
(дворник Кузьмич)

